SciTech-Chemistry(化学)-电解: 电化学之"Electrolysis(电解)"化学工艺及应用
SciTech-Chemistry(化学)-电解: 电化学之"Electrolysis(电解)"化学工艺及应用
Electrolysis(电解) 是将 电流 通过 电解质溶液或熔融态电解质,在 阴极和阳极 上引起 氧化还原反应 的过程,
通电时, 阴阳两电极都生成新物质:
- 电解质 的 阳离子 移向 阴极,
吸收电子,发生还原反应,生成新物质; - 电解质 的 阴离子 移向阳极,
放出电子,发生氧化反应,生成新物质。 - 能量转换的视角: 电解池 是将 电能 转化为 化学能 的装置。
即: 电解 是在电极(作为电子导体)与 电解质(作为离子导体) 的 界面上 发生 电化学氧化还原反应 合成 化学品 的过程.
用途: 合成高纯物质的制造, 以及材料表面处理。
最常见应用: "电化学电池" 在 "充电时(外加DC电压)"发生"电解(充电)"的过程。
定义
电解是将 电流 通过 电解质溶液或熔融态电解质,在阴极和阳极上 引起 氧化还原反应 的过程。
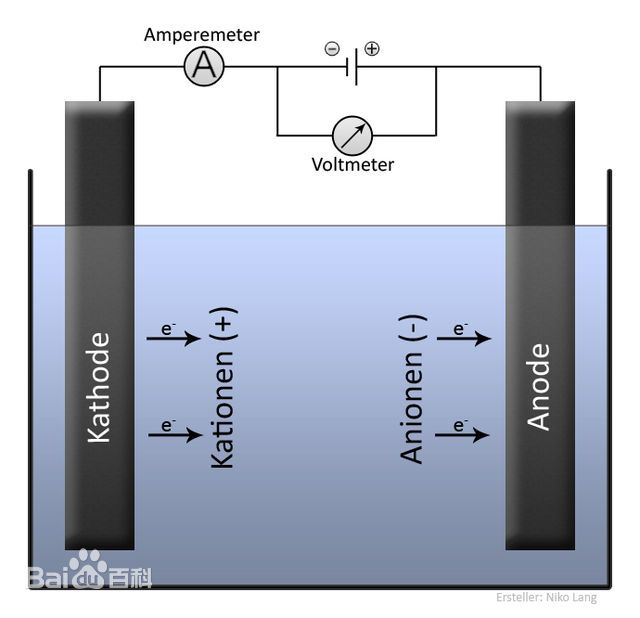
电解过程是在 电解池 进行的。电解池是由分别浸没在溶液(含有正、负离子)的阴、阳两个电极构成。
 |
 |
电流流进负电极(阴极),溶液的:
- 正离子(带正电荷)迁移到 阴极,并与电子结合,产出 电中性 的 元素或分子;
- 负离子(带负电荷) 迁移到 阳极,释放(给)出电子,产出 电中性 的 元素或分子。
电解过程必须具备: 电解质、电解槽、直流供电系统、分析控制系统和对产品的分离回收装置。
电解过程应:
- 尽可能用较低成本的原料,
- 提高反应的选择性,
- 减少副产物生成,
- 缩短生产工序,
- 便于产品回收和净化。
电解过程已广泛用于有色金属冶炼、氯碱工业和无机盐生产以及有机化学工业。 [1]
电解的历史
- 1807年, 英国科学家 H.戴维 电解 熔融苛性碱 制取钾、钠, 开拓获取 高纯度物质 的新领域。
- 1833年, 英国物理学家 M.法拉第 提出 电化学当量定律(即法拉第第一、第二定律)。
- 1886年, 美国工业化学家 C.M.霍尔 电解制铝 成功。
- 1890年,第一个 电解氯化钾 制取氯气 的 工厂在 德国投产。
- 1893年,开始使用 隔膜电解法,用 食盐溶液 制 烧碱。
- 1897年,水银电解法 制 烧碱 实现工业化。
至此,电解法成为化学工业和冶金工业的一种重要生产方法。 - 1937年,阿特拉斯化学工业公司 实现用 电解法 由 葡萄糖 生产 山梨醇及甘露糖醇的工业化,
这是第一个大规模用电解法生产有机化学品的过程。 - 1969年又开发了由 丙烯腈 电解二聚 生产 己二腈 的工艺。
电解原理
电解质的离子常处于无秩序的运动,通直流电后,离子作定向运动。
- 阳离子向阴极移动,在阴极得到电子,被还原;
- 阴离子向阳极移动,在阳极失去电子,被氧化。
举例,水电解过程,
- OH-在阳极失去电子,被氧化成氧气放出;
- H+在阴极得到电子,被还原成氢气放出。
所得到的氧气和氢气,即为水电解过程的产品。
电解时,在电极上析出的产物与电解质溶液之间形成电池,其电动势在数值上等于电解质的理论电解电压。
此理论电解电压可由能斯特方程计算:
上式的:
E0为标准电极电位(R为气体常数,等于8.314J/(K·mol);
T为温度(K);
n为电极反应中得失电子数;
F为法拉第常数,等于96500 C/mol;
α1、α2分别为还原态和氧化态物质的活度。
- 整个电解过程 的 理论电解电压 为两个电极理论电解电压之差。
甚至 实际电解电压的高低 决定 电解条件 的放电 物质.
还以 水溶液电解 为例,实际电解电压的高低 决定: 是 电解质电离的正负离子 还是 水电离的H+和OH- 在 电极上 放电, - 实际电解电压 为 理论电解电压 与 超电 压 之和。
影响超电压的因素很多,有电极材料和电极间距、电解液温度、浓度、pH等。
例如在氯碱生产过程(用碳电极),
- 浓的食盐水溶液电解时,实际上是“电解质的电解”:
- 阴极放出氢气,同时产生氢氧化钠,
- 阳极放出氯气;
- 稀的食盐水溶液电解时,实际上是“水的电解”:
- 阴极放出氢气,同时产生氢氧根,与水的钠离子结合为氢氧化钠,
- 阳极放出氧气,同时产生氢离子,与水氯离子结合产生氯化氢,溶于水产生盐酸。
- 氢氧化钠 与 盐酸 反应生成 氯化钠和水。
因此:
稀的食盐水溶液 电解反应为 电解水反应,产生氢气和氧气。
原理分析
以氯化铜(CuCl2)溶液的电解为例:
CuCl2是强电解质且易溶于水,在水溶液电离生成 Cu2+和Cl-。
- 通电前,Cu2+和Cl-在水里自由地移动着;
- 通电后,这些自由移动着的离子,在电场作用下,改作定向移动。
溶液的带正电的Cu2+向阴极移动,带负电的氯离子向阳极移动。- 在阴极,铜离子获得电子而还原成铜原子覆盖在阴极上;
阴极:Cu2++2e-=Cu - 在阳极,氯离子失去电子而被氧化成氯原子,并两两结合成氯气分子,由阳极放出。
阳极:2Cl--2e-=Cl2↑
- 在阴极,铜离子获得电子而还原成铜原子覆盖在阴极上;
两极放电顺序
阴离子:S2->I->Br->Cl->OH->SO42->F-
阳离子:Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+
注:铝离子,镁离子,钠离子,钙离子,钾离子 得电子能力 远远小于 氢离子得电子能力,
所以, 这些离子 不能在水溶液为条件 在电极(阴极)析出, 因为水溶液的水有;氢离子 和 氧离子。
但是, 在熔融状态 可以放电。
三价铁离子在阴极上得电子生成亚铁离子,而非铁单质。
电解质
电解质是指在 水溶液或熔融状态下 能够 导电 的化合物。例如酸、碱和大部份盐等。
- 凡在上述情况下 不能导电 的 化合物 叫 非电解质,例如蔗糖、酒精等。
- 单质,混合物不管在水溶液或熔融状态 能够导电与否,都不是电解质。
- 化合物导电的前提:其内部存在着自由移动的阴阳离子。
离子化合物, 在水溶液或熔化状态下能导电;
共价化合物, 一些也能在水溶液导电(如HCl)。
强电解质一般有强酸、强碱,大多数盐、活泼金属的氧化物、氢化物。
弱电解质一般有弱酸、弱碱。另外,水是极弱电解质。
注:能导电的不一定是电解质,
判断某化合物是否是电解质,不能只凭它在水溶液的 导电与否,还需要进一步考察其晶体结构和化学键的性质等因素。
例如,判断硫酸钡、碳酸钙和氢氧化铁是否为电解质。
- 硫酸钡难溶于水,溶液的离子浓度很小,其水溶液不导电,似乎为非电解质。但溶于水的那小部分却几乎完全电离。因此,硫酸钡是电解质。
- 碳酸钙和硫酸钡具有相类似的情况,也是电解质。
结构上看,对其他难溶盐,只要是离子型化合物或强极性共价型化合物,尽管难溶,也是电解质。 - 氢氧化铁的情况则比较复杂,Fe与OH之间的化学键带有共价性质,它的溶解度比硫酸钡还要小;
而溶于水的部分,其少部分又有可能形成胶体,其余亦能电离成离子。
但氢氧化铁也是电解质。
判断氧化物是否为电解质,也要作具体分析。
非金属氧化物如SO2、SO3、P2O5、CO2等,它们是共价型化合物,液态时不导电,所以不是电解质。
有些氧化物在水溶液即便能导电,但也不是电解质。
因为这些氧化物与水反应生成了新的能导电的物质,溶液导电的不是原氧化物,
如SO2本身不能电离,而它和水反应,生成亚硫酸,亚硫酸为电解质。
金属氧化物如Na2O,MgO,CaO,Al2O3等是离子化合物,它们在熔化状态下能够导电,因此是电解质。
需要注意的是,氯化铝(AlCl3)是电解质,但是, 是共价化合物 而不是 离子化合物。
可见,电解质包括离子型或强极性共价型化合物;非电解质包括弱极性或非极性共价型化合物。
电解质水溶液能够导电,是因电解质可以离解成离子。至于物质在水中能否电离,是由其结构决定的。
因此,由物质结构识别电解质与非电解质是问题的本质。
另外,有些能导电的物质,如铜、铝等不是电解质。
因它们并不是能导电的化合物,而是单质,不符合电解质的定义。 [2]
在氯化铜电解的过程,没有提到溶液里的H+和OH-,其实H+和OH-虽少,但的确是存在的,只是他们没有参加电极反应。
也就是, 在氯化铜溶液,除Cu2+和Cl-外,还有H+和OH-,电解时,
移向阴极的离子有Cu2+和H+,因为在这样的实验条件下Cu2+比H+容易得到电子,所以Cu2+在阴极上得到电子析出金属铜。
移向阳极的离子有OH-和Cl-,因为在这样的实验条件下,Cl-比OH-更容易失去电子,所以Cl-在阳极上失去电子,生成氯气。
- 放电: 阳离子得到电子 或 阴离子失去电子 而使 离子所带电荷数目降低 的过程。
- 电极 的 惰性 与 活性
- 惰性电极 是一般在 通电条件 不发生化学反应的, 如用石墨、金、铂等还原性很弱的材料制做的电极。
- 活性电极 是 做电解池的阳极时 先于其他物质发生氧化反应的。如用铁、锌、铜、银等还原性较强材料制做的电极.
- 在一般的电解条件下,
- 水溶液含有多种阳离子时,它们在阴极上放电的先后顺序是:
Ag+ > Hg2+ > Fe3+ > Cu2+ > H+ > Pb2+ > Sn2+ > Fe2+ > Zn2+ > Al3+ > Mg2+ > Na+ > Ca2+ > K+; - 水溶液含有多种阴离子时,它们的惰性阳极上放电的先后顺序是:
S2- > I- > Br-> Cl- > OH- > 含氧酸根 > F-。
分析惰性电极电解反应的一般方法步骤:- 分析电解质水溶液的组成,找全离子并分为阴、阳两组;
- 分别对阴、阳离子排出放电顺序,写出两极上的电极反应式;
- 合并两个电极反应式得出电解反应的总化学方程式或离子方程式。
- 水溶液含有多种阳离子时,它们在阴极上放电的先后顺序是:
类型
电解方式按电解质状态可分为水溶液电解和熔融盐电解两大类。
- 水溶液电解:主要有:
电解水制取氢气和氧气;
电解氯化钠(钾)水溶液制氢氧化钠(钾)和氯气、氢气;
电解氧化法制各种氧化剂,如过氧化氢、氯酸盐、高氯酸盐、高锰酸盐、过硫酸盐等;
电解还原法如丙烯腈电解制己二腈;
湿法电解制金属如锌、镉、铬、锰、镍、钴等;
湿法电解精制金属如铜、银、金、铂等。
此外,电镀、电抛光、阳极氧化等都是通过水溶液电解来实现的。 - 熔融盐电解:主要包括:
金属冶炼,如铝、镁、钙、钠、钾、锂、铍等;
金属精制,如铝、钍等;
此外,还有将熔融氟化钠电解制取元素氟等。
电解所用主体设备电解槽的形式,可分为隔膜电解槽和无隔膜电解槽两类。
隔膜电解槽又可分为均向膜(石棉绒)、离子膜及固体电解质膜(如β-Al2O3)等形式;
无隔膜电解槽又分为水银电解槽和氧化电解槽等。
电极上发生的过程,可分简单电子传递、气体释放、金属腐蚀、金属析出、氧化物生成和有机物二聚等类型。
用途
电解广泛应用于冶金工业,如:
矿石或化合物提取金属(电解冶金)或提纯金属(电解提纯),
以溶液沉积出金属(电镀)。
电解是一种非常强有力的促进氧化还原反应的手段,许多很难进行的氧化还原反应,都可以通过电解来实现。
如可将熔融的氟化物在阳极上氧化成单质氟,熔融的锂盐在阴极上还原成金属锂。
电解工业在国民经济有重要作用,以下都是通过电解实现的:
- 许多有色金属(如钠、钾、镁、铝等)和稀有金属(如锆、铪等)的冶炼,
- 金属(如铜、锌、铅等)的精炼,
- 基本化工产品(如氢、氧、烧碱、氯酸钾、过氧化氢、乙二腈等)的制备,
- 还有电镀、电抛光、阳极氧化等。
影响因素
判断电解过程优劣的主要标准是单位产品用电量,其高低取决于 电解过程的 电流效率和电压效率。
电流效率
单位产品的理论用电量与实际用电量之比。
理论用电量可用法拉第定律计算:
此式表明,电解时析出的物质量q:
与析出物质的原子量m、电流强度I及电解时间t成正比,
而与电解过程 得失电子数n及法拉第常数F成反比。
在正常情况下电流效率比较高。
电压效率
电解时电解质的理论电解电压与实际电解电压之比。后者即是电解槽的槽电压。
槽电压是理论电解电压、超电压和输电导体电压损失之和。
影响槽电压大小的因素很多,前述影响超电压的因素外,还有导线与电极之间的接触电压、隔膜材料、电解槽结构、电流密度等。
槽电压通常远大于理论电解电压,导致电压效率很低。
因此,降低超电压和输电导体的电压损失是提高电压效率的关键。
多年来,人们围绕这一问题进行了多方面的研究,不断改善电解槽结构和电极材料。- 在电极材料方面的研究,集中于电极材质的选择。
在阳极方面由石墨电极发展为钛电极、钛铂铱电极、钛钌电极及其他非钌电极。
此外,还开发了有许多特殊用途的二氧化锰电极、二氧化铅电极等。 - 在阴极方面,由铁阴极发展成多孔阴极。
近年来,又发展了一种新型氧气电极过程,将燃料电池的原理应用于电解工业。
无论是阴极或阳极,都有在电极基体表面涂加活性物质的趋势,
目的是使电极具有催化作用(称为电催化法),通过降低槽电压以达到节省电能的目的。- 在电极材料方面的研究,集中于电极材质的选择。
SciTech-Chemistry(化学)-电解: 电化学之"Electrolysis(电解)"化学工艺及应用的更多相关文章
- 第三届材料化学与复合材料国际学术会议(MCCM 2022)
大会官网:http://www.meeting-mccm.org/ 大会时间:2022年12月16-18日 大会地点:中国-珠海 截稿日期:详情见官网(2022年10月14日) 接受/拒稿通知:投稿后 ...
- ChemDraw中化学信息怎么通过Excel搜索
用户可以通过ChemDraw for Excel插件功能在Office Excel中建立ChemOffice菜单将ChemOffice和Excel结合使用,使用电子表格的最大优势之一就是可以清晰查看并 ...
- 可以将化学结构NMR图谱这样导入Word
在化学各个领域中,大家常常会用到ChemDraw化学绘图软件来绘制各种图形,ChemDraw因其出色的功能在全球范围内深受欢迎,但是一些用户朋友对于一些功能还不是很了解,需要通过一些教程来了解如何操作 ...
- sciencesoftware科学软件
软件名称 软件分类 二级分类 更新日期 下载 GMS(Groundwater Modeling Solution) 10 地球地理软件 水资源 2014-09-28 下载 Data Desk 7 经济 ...
- 关于MIM金属注射成型技术知识大全
1.什么是MIM MIM即(Metal Injection Molding)是金属注射成型的简称.是将金属粉末与其粘结剂的增塑混合料注射于模型中的成形方法.它是先将所选粉末与粘结剂进行混合,然后将混合 ...
- 开关电源PCB设计中的布线技巧
开关电源PCB设计中的布线技巧关键字:布线 开关电源 走线 一.引言 开关电源是一种电压转换电路,主要的工作内容是升压和降压,广泛应用于现代电子产品.因为开关三极管总是工作在 “开” 和“关” 的状态 ...
- TEXT 5 Stuff of dreams
TEXT 5 Stuff of dreams 梦想的精粹 Feb 16th 2006 | CORK AND LONDON From The Economist print edition (译者注:本 ...
- 使用LM386制作Arduino音乐播放器
在我们的项目中添加声音或音乐总是会使其看起来更酷一些,听上去更有吸引力.特别是如果您使用的是Arduino开发板,并且有很多空余的引脚,只需要添加一个SD卡模块和一个普通的扬声器即可轻松添加音效.在本 ...
- 【雕爷学编程】Arduino动手做(58)---SR04超声波传感器
37款传感器与执行器的提法,在网络上广泛流传,其实Arduino能够兼容的传感器模块肯定是不止这37种的.鉴于本人手头积累了一些传感器和执行器模块,依照实践出真知(一定要动手做)的理念,以学习和交流为 ...
- 记lrd的高二上学期第五次调研考试
河北某某中学的调研考试其实是很好玩的经历呢.可惜没有太多机会了. 背景: NOIP2016回来之后没有好好学文化课-.自习能翘就翘了,衡中特产学案自助没有好好写(说来我好像从来没被老师查到过,上课写学 ...
随机推荐
- thinkphp里__PUBLIC__的使用
1.默认值 __PUBLIC__常量默认指向当前项目根目录下的pulic目录, 例如:www下有一个blog项目目录,blog下一般有application.Home.public.Thinkphp ...
- php 设置友好时间
public static function formatTime($time){ if (is_int($time)) { $time = intval($time); } elseif ($tim ...
- C#/.NET/.NET Core技术前沿周刊 | 第 36 期(2025年4.21-4.27)
前言 C#/.NET/.NET Core技术前沿周刊,你的每周技术指南针!记录.追踪C#/.NET/.NET Core领域.生态的每周最新.最实用.最有价值的技术文章.社区动态.优质项目和学习资源等. ...
- coreybutler/nvm-windows 简单使用
目录 nvm是什么 安装 简单命令 nvm是什么 Windows电脑node.js管理器.可以方便node.js的安装与切换. 最新版本1.1.11 coreybutler/nvm-windows 有 ...
- 如何反向绘制出 .NET程序 异步方法调用栈
一:背景 1. 讲故事 这个问题源于给训练营里的一位朋友分析的卡死dump,在分析期间我需要知道某一个异步方法的调用栈,但程序是 .framework 4.8 ,没有sos后续版本独有的 !dumpa ...
- Python Set | update()
Python update() function in set adds elements from a set (passed as an argument) to the set. Syntax ...
- MCP SSE交互完整过程
有关MCP的介绍文章很多,本文不细说,做一个时序图将完整过程说清楚.MCP协议主要通过两种技术实现:标准输入输出(stdio)和服务器发送事件(SSE),stdio(标准输入输出)是MCP协议在本地或 ...
- ciscn暨长城杯 广东赛区 ISW阶段应急响应
ciscn暨长城杯 广东赛区 ISW阶段应急响应 题目介绍 小路是一名网络安全网管,据反映发现公司主机上有异常外联信息,据回忆前段时间执行过某些更新脚本(已删除),现在需要协助小路同学进行网络安全应急 ...
- sqlite:No module named _sqlite3
执行代码报错:"sqlite:No module named _sqlite3" 执行环境说明 某台服务器上执行DrissionPage相关程序报错,本机没有问题. 解决说明 本机 ...
- Manim中三种函数图像类的比较
在 Manim 库中,FunctionGraph.ImplicitFunction 和 ParametricFunction 都是用于绘制函数图像的类,但它们的适用场景.输入形式和实现方式有显著区别. ...
