单细胞分析实录(8): 展示marker基因的4种图形(一)
今天的内容讲讲单细胞文章中经常出现的展示细胞marker的图:tsne/umap图、热图、堆叠小提琴图、气泡图,每个图我都会用两种方法绘制。
使用的数据来自文献:Single-cell transcriptomics reveals regulators underlying immune cell diversity and immune subtypes associated with prognosis in nasopharyngeal carcinoma. 去年7月发表在Cell Research上的关于鼻咽癌的文章,数据下载:https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE150430
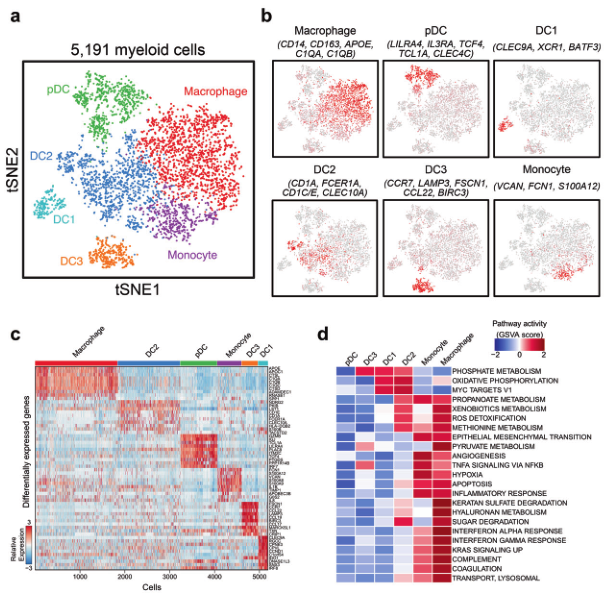
髓系细胞数量相对少一些,为了方便演示,选它作为例子。
library(Seurat)
library(tidyverse)
library(harmony)
Myeloid=read.table("Myeloid_mat.txt",header = T,row.names = 1,sep = "\t",stringsAsFactors = F)
Myeloid_anno=read.table("Myeloid_anno.txt",header = T,sep = "\t",stringsAsFactors = F)
导入数据的时候需要注意一个地方:从cell ranger得到的矩阵,每一列的列名会在CB后面加上"-1"这个字符串,在R里面导入数据时,会自动转化为".1",在做匹配的时候需要注意一下。我已经提前转换为"_1"
> summary(as.numeric(Myeloid["CD14",]))
Min. 1st Qu. Median Mean 3rd Qu. Max.
0.000 0.000 0.689 1.080 2.111 4.500
> summary(as.numeric(Myeloid["PTPRC",]))
Min. 1st Qu. Median Mean 3rd Qu. Max.
0.000 1.200 1.681 1.607 2.124 3.520
考虑到下载的表达矩阵,表达值都不是整数,且大于0,推测该矩阵已经经过了标准化,因此下面的流程会跳过这一步
0. Seurat流程
我们直接把注释结果赋值到mye.seu@meta.data矩阵中,后面省去聚类这一步
mye.seu=CreateSeuratObject(Myeloid)
mye.seu@meta.data$CB=rownames(mye.seu@meta.data)
mye.seu@meta.data=merge(mye.seu@meta.data,Myeloid_anno,by="CB")
rownames(mye.seu@meta.data)=mye.seu@meta.data$CB
#替代LogNormalize这一步
mye.seu[["RNA"]]@data=mye.seu[["RNA"]]@counts
mye.seu <- FindVariableFeatures(mye.seu, selection.method = "vst", nfeatures = 2000)
mye.seu <- ScaleData(mye.seu, features = rownames(mye.seu))
mye.seu <- RunPCA(mye.seu, npcs = 50, verbose = FALSE)
mye.seu=mye.seu %>% RunHarmony("sample", plot_convergence = TRUE)
mye.seu <- RunUMAP(mye.seu, reduction = "harmony", dims = 1:20)
mye.seu <- RunTSNE(mye.seu, reduction = "harmony", dims = 1:20)
#少了聚类
DimPlot(mye.seu, reduction = "tsne", group.by = "celltype", pt.size=1)+theme(
axis.line = element_blank(),
axis.ticks = element_blank(),axis.text = element_blank()
)
ggsave("tsne1.pdf",device = "pdf",width = 17,height = 14,units = "cm")
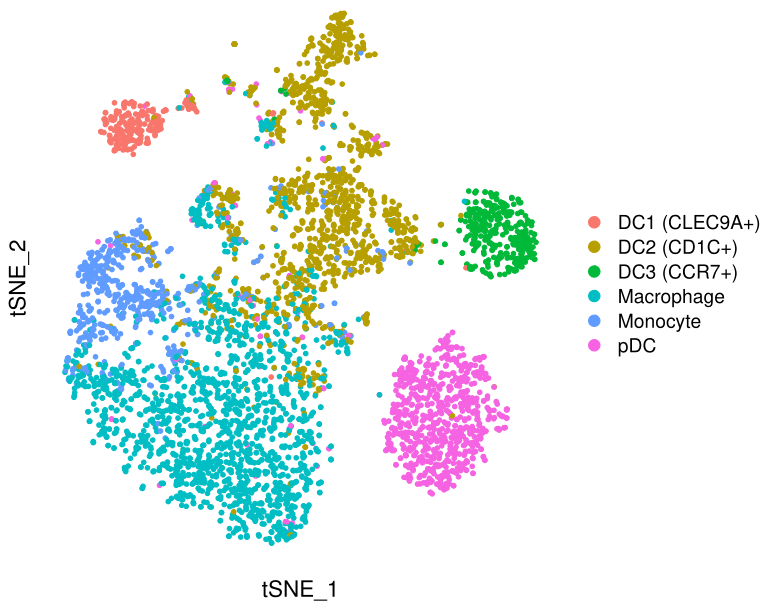
基本符合原图,三个亚群分得开,三个亚群分不开。
接下来,我用4种方式展示marker基因,这些基因可以在文献的补充材料里面找到。
1. tsne展示marker基因
FeaturePlot(mye.seu,features = "CCR7",reduction = "tsne",pt.size = 1)+
scale_x_continuous("")+scale_y_continuous("")+
theme_bw()+ #改变ggplot2的主题
theme( #进一步修改主题
panel.grid.major = element_blank(),panel.grid.minor = element_blank(), #去掉背景线
axis.ticks = element_blank(),axis.text = element_blank(), #去掉坐标轴刻度和数字
legend.position = "none", #去掉图例
plot.title = element_text(hjust = 0.5,size=14) #改变标题位置和字体大小
)
ggsave("CCR7.pdf",device = "pdf",width = 10,height = 10.5,units = "cm")
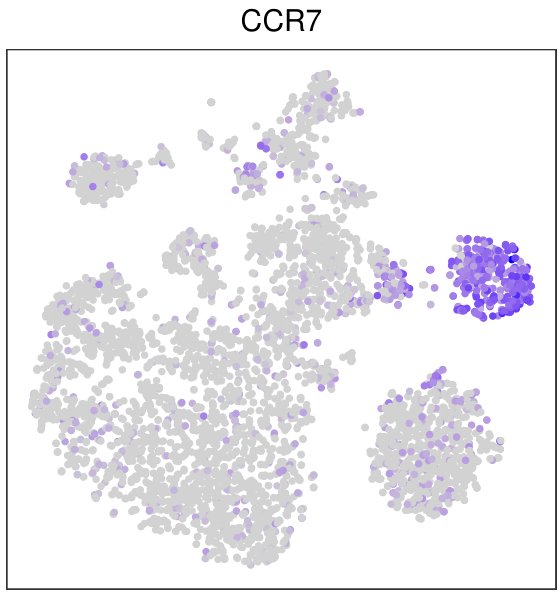
另一种方法就是把tsne的坐标和基因的表达值提取出来,用ggplot2画,其实不是很必要,因为FeaturePlot也是基于ggplot2的,我还是演示一下
mat1=as.data.frame(mye.seu[["RNA"]]@data["CCR7",])
colnames(mat1)="exp"
mat2=Embeddings(mye.seu,"tsne")
mat3=merge(mat2,mat1,by="row.names")
#数据格式如下:
> head(mat3)
Row.names tSNE_1 tSNE_2 exp
1 N01_AAACGGGCATTTCAGG_1 5.098727 32.748145 0.000
2 N01_AAAGATGCAATGTAAG_1 -24.394040 26.176422 0.000
3 N01_AACTCAGGTAATAGCA_1 11.856730 8.086553 0.000
4 N01_AACTCAGGTCTTCGTC_1 10.421878 12.660407 0.000
5 N01_AACTTTCAGGCCATAG_1 33.555756 -10.437406 1.606
6 N01_AAGACCTTCGAATGGG_1 -23.976967 11.897753 0.738
mat3%>%ggplot(aes(tSNE_1,tSNE_2))+geom_point(aes(color=exp))+
scale_color_gradient(low = "grey",high = "purple")+theme_bw()
ggsave("CCR7.2.pdf",device = "pdf",width = 13.5,height = 12,units = "cm")

用ggplot2的好处就是图形修改很方便,毕竟ggplot2大家都很熟悉
2. 热图展示marker基因
画图前,需要给每个细胞一个身份,因为我们跳过了聚类这一步,此处需要手动赋值
Idents(mye.seu)="celltype"
library(xlsx)
markerdf1=read.xlsx("ref_marker.xlsx",sheetIndex = 1)
markerdf1$gene=as.character(markerdf1$gene)
# 这个表格整理自原文的附表,选了53个基因
#数据格式
# > head(markerdf1)
# gene celltype
# 1 S100B DC2(CD1C+)
# 2 HLA-DQB2 DC2(CD1C+)
# 3 FCER1A DC2(CD1C+)
# 4 CD1A DC2(CD1C+)
# 5 PKIB DC2(CD1C+)
# 6 NDRG2 DC2(CD1C+)
DoHeatmap(mye.seu,features = markerdf1$gene,label = F,slot = "scale.data")
ggsave("heatmap.pdf",device = "pdf",width = 23,height = 16,units = "cm")
label = F不在热图的上方标注细胞类型,
slot = "scale.data"使用scale之后的矩阵画图,默认就是这个

接下来用pheatmap画,在布局上可以自由发挥
library(pheatmap)
colanno=mye.seu@meta.data[,c("CB","celltype")]
colanno=colanno%>%arrange(celltype)
rownames(colanno)=colanno$CB
colanno$CB=NULL
colanno$celltype=factor(colanno$celltype,levels = unique(colanno$celltype))
先对细胞进行排序,按照celltype的顺序,然后对基因排序
rowanno=markerdf1
rowanno=rowanno%>%arrange(celltype)
提取scale矩阵的行列时,按照上面的顺序
mat4=mye.seu[["RNA"]]@scale.data[rowanno$gene,rownames(colanno)]
mat4[mat4>=2.5]=2.5
mat4[mat4 < (-1.5)]= -1.5 #小于负数时,加括号!
下面就是绘图代码了,我加了分界线,使其看上去更有区分度
pheatmap(mat4,cluster_rows = F,cluster_cols = F,
show_colnames = F,
annotation_col = colanno,
gaps_row=as.numeric(cumsum(table(rowanno$celltype))[-6]),
gaps_col=as.numeric(cumsum(table(colanno$celltype))[-6]),
filename="heatmap.2.pdf",width=11,height = 7
)
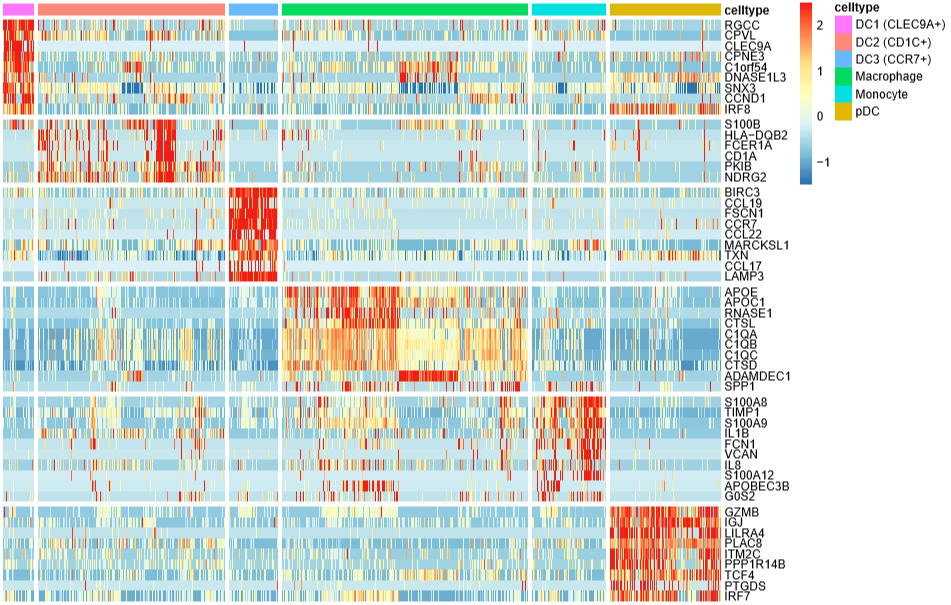
先写到这儿吧(原本以为能写完的),剩下的气泡图、堆叠小提琴图改天再补上。
因水平有限,有错误的地方,欢迎批评指正!
单细胞分析实录(8): 展示marker基因的4种图形(一)的更多相关文章
- 单细胞分析实录(9): 展示marker基因的4种图形(二)
在上一篇中,我已经讲解了展示marker基因的前两种图形,分别是tsne/umap图.热图,感兴趣的读者可以回顾一下.这一节我们继续学习堆叠小提琴图和气泡图. 3. 堆叠小提琴图展示marker基因 ...
- 【代码更新】单细胞分析实录(20): 将多个样本的CNV定位到染色体臂,并画热图
之前写过三篇和CNV相关的帖子,如果你做肿瘤单细胞转录组,大概率看过: 单细胞分析实录(11): inferCNV的基本用法 单细胞分析实录(12): 如何推断肿瘤细胞 单细胞分析实录(13): in ...
- 【代码更新】单细胞分析实录(21): 非负矩阵分解(NMF)的R代码实现,只需两步,啥图都有
1. 起因 之前的代码(单细胞分析实录(17): 非负矩阵分解(NMF)代码演示)没有涉及到python语法,只有4个python命令行,就跟Linux下面的ls grep一样的.然鹅,有几个小伙伴不 ...
- 单细胞分析实录(5): Seurat标准流程
前面我们已经学习了单细胞转录组分析的:使用Cell Ranger得到表达矩阵和doublet检测,今天我们开始Seurat标准流程的学习.这一部分的内容,网上有很多帖子,基本上都是把Seurat官网P ...
- 单细胞分析实录(4): doublet检测
最近Cell Systems杂志发表了一篇针对现有几种检测单细胞测序doublet的工具的评估文章,系统比较了常见的例如Scrublet.DoubletFinder等工具在检测准确性.计算效率等方面的 ...
- 单细胞分析实录(3): Cell Hashing数据拆分
在之前的文章里,我主要讲了如下两个内容:(1) 认识Cell Hashing:(2): 使用Cell Ranger得到表达矩阵.相信大家已经知道了cell hashing与普通10X转录组的差异,以及 ...
- 单细胞分析实录(18): 基于CellPhoneDB的细胞通讯分析及可视化 (上篇)
细胞通讯分析可以给我们一些细胞类群之间相互调控/交流的信息,这种细胞之间的调控主要是通过受配体结合,传递信号来实现的.不同的分化.疾病过程,可能存在特异的细胞通讯关系,因此阐明这些通讯关系至关重要. ...
- 单细胞分析实录(19): 基于CellPhoneDB的细胞通讯分析及可视化 (下篇)
在上一篇帖子中,我介绍了CellPhoneDB的原理.实际操作,以及一些值得注意的地方.这一篇继续细胞通讯分析的可视化. 公众号后台回复20210723获取本次演示的测试数据,以及主要的可视化代码. ...
- 单细胞分析实录(2): 使用Cell Ranger得到表达矩阵
Cell Ranger是一个"傻瓜"软件,你只需提供原始的fastq文件,它就会返回feature-barcode表达矩阵.为啥不说是gene-cell,举个例子,cell has ...
随机推荐
- PyQt学习随笔:Qt中Model/View相关的主要类及继承关系
View相关类类继承关系: Model相关类类继承关系:
- 【Vue】 axios同步执行多个请求
问题 项目中遇到一个需求,在填写商品的时候,选择商品分类后,加载出商品分类的扩展属性. 这个扩展属性有可能是自定义的数据字典里的单选/多远. 要用第一个axios查询扩展属性,第二个axios 从第一 ...
- 推荐系统实践 0x0c FM系列
逻辑回归(LR) 在介绍FM系列之前,我想首先简单介绍一下逻辑回归.通常来说,逻辑回归模型能够综合利用更多的信息,如用户.物品.上下文等多种不同的特征,生成更为全面的结果.另外,逻辑回归将推荐问题看成 ...
- Kubernetes的Local Persistent Volumes使用小记
欢迎访问我的GitHub https://github.com/zq2599/blog_demos 内容:所有原创文章分类汇总及配套源码,涉及Java.Docker.Kubernetes.DevOPS ...
- 网络拓扑实例13:IPv4静态路由与NQA联动简介
组网图形 IPv4静态路由与NQA联动简介 网络质量分析NQA(Network Quality Analysis)是一种实时的网络性能探测和统计技术,可以对响应时间.网络抖动.丢包率等网络信息进行统计 ...
- 题解-CTS2019 珍珠
题面 CTS2019 珍珠 有 \(n\) 个在 \([1,d]\) 内的整数,求使可以拿出 \(2m\) 个整数凑成 \(m\) 个相等的整数对的方案数. 数据范围:\(0\le m\le 10^9 ...
- 排序算法-Java实现快速排序算法
- 从函数到包的Python代码层次
代码层次 Python是一门脚本语言,新建一个.py文件,写点代码,就可以跑起来了,无论放哪都可以.比如where.py文件: print("Where am I?") 那么问题来 ...
- IOS实现自动定位和手动选择城市功能
IOS自动定位使用的是高德地图SDK 在高德开放平台http://lbs.amap.com/api/ios-sdk/down/ 下载2D地图SDK和搜索SDK 将SDK导入工程内 按照高德的配置说明进 ...
- 网站开发学习Python实现-Django学习-总结(6.1.2)
@ 目录 1.MVT 2.模型 3.视图 4.模板 5.常用的命令 6.pycharm创建django工程 关于作者 1.MVT 项目结构如下,其中项目同名文件夹为配置文件 每一个项目有多个应用(未考 ...
